今回はエンタルピーについて解説をしていきます。
エンタルピー
エンタルピー(H)とは
エンタルピー(H)とはズバリ「熱量」のことを言います。
※日常的に使う「熱」のイメージに近いです。
皆さんの体で例えるのであれば、体内にある熱エネルギーの総量であると思ってください。
イメージはこんな形です。
<図1>

熱(q)との違いは?
エンタルピーは熱量であると知ったと同時に、こんなことを思った方もいるかと思います。「熱ってqという文字を使ってるのを見たことがあるんたけどな~」と思った方もいますよね。
おっしゃる通り一般的に熱は「q」で表します。私も学生時代このあたりでリタイアしたことあります。
なのでここではエンタルピーとの違いについて説明していきます。
違いについては大きく2つあります。
- エンタルピーは主に定圧過程条件下で扱う用語
- エンタルピー(H)は「熱量」! ※熱(q)とは違う
エンタルピーは主に定圧過程条件下で扱う用語
エンタルピーを考えていく際にはどの条件下なのかを考える必要があります。
条件には以下の種類などがあります。
- 定圧過程
- 定容過程
- 等温過程
- 断熱過程
それぞれの過程について話をするとまたややこしくなるので、それはまた別の機会にしますが、今回大事なのは、この条件によって熱(q)の扱いが異なるということです。
皆さんが普段生活している、大気圧下(定圧過程)で扱いやすい熱(q)の用語としてエンタルピーが存在していると思ってください。
エンタルピー(H)は「熱量」! ※熱(q)とは違う
エンタルピーとは「熱量」のことです。
冒頭でエンタルピーは体で例えた時の、体内にある熱エネルギーの総量であるとお話ししました。これが体内の「熱量」です。
一方で「熱」というのは体内に外部から入ってくる熱エネルギーのことです。
どちらも熱エネルギーでることに変わりはないですが、区別しておくほう吉です。
イメージはこんな感じです。
<図2>
おまけ
最後におまけとして、2つほどテスト等に関係する内容を記載します。
ΔH=q が成立する。(定圧条件下において)
定圧条件下のおいては、ΔH=q が成立します。 ※ただしHはエンタルピー、qは熱を表す。
公式にある「Δ」これは「デルタ」と読み、変化量を表します。
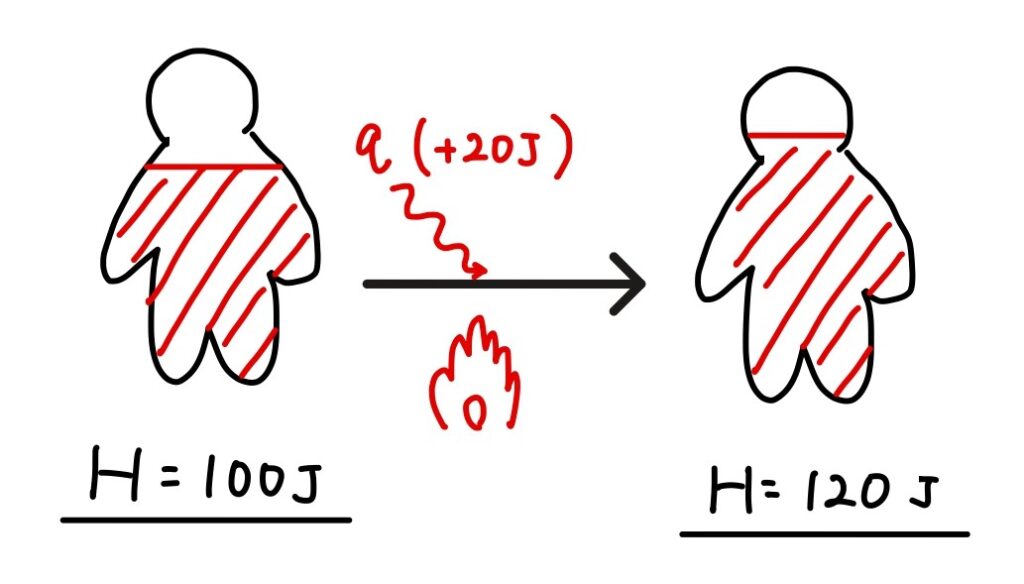
例えば、お風呂に入る前の体内のエンタルピーが100Jだったとします。お風呂に入った後エンタルピーが120Jになった場合。この人のエンタルピー変化(ΔH)は+20Jということになります。これが変化量です。
この例を別視点でも考えると、お風呂に入ることで体内には20Jの熱(q)が入ってきとも考えられます。
つまり入ってきた熱(q)の分だけ体内のエンタルピー(H)が増加するので、ΔH=q が成立します。
公式から考えると難しく感じる部分も用語の意味を理解すると当たり前のことを言っていることが分かりますね!!
ちなみに
熱が入ってくる反応(吸熱反応)の場合→ΔH>0(変化量が正の値)
熱が出ていく反応(発熱反応)の場合→ΔH<0(変化量が負の値)
となります。ΔHの値で吸熱反応か発熱反応か判断できるとよいですね!
エンタルピー(H)は状態関数、熱(q)は経路関数
状態関数や経路関数という用語を聞いたことはありますか?
いわば物理学で出てくる用語(例えば質量、体積、仕事など)を分類する用語だと思ってください。
関数には大きく2つあり、状態関数と経路関数があります。
ざっくり以下のような性質です。
- 状態関数→「現在の状態」だけで値が決まる物理量のこと
- 経路関数→「どのような道筋を通ったか」によって値が変わる物理量のこと
図2を見るとイメージがしやすいと思います。
エンタルピーは現在の体内にある熱の総量で、現在の状態をだけで決まります。 (過去のエンタルピーは関係なく、今どのくらいかを表しています。)そのため「状態関数」に分類されます。
一方で熱は体内に入ってくる際の経路に関係します。そのため「経路関数」に分類されます。
まとめ
今回はエンタルピーについて解説しました。
エンタルピーの特徴を以下に簡単にまとめます。
- エンタルピーは「熱量」を示す
- 主に定圧過程条件下で扱う用語
- エンタルピーの変化量(ΔH)は入ってくる熱(q)の値に等しい(ΔH=q)
- エンタルピーは状態関数で現在の状態のみによって決まる値
以上です。
皆さんの学習にぜひお役立てください。


コメント